He estado pensando cómo podía aportar algo de información potencialmente útil y de interés, desde mi experiencia como genetista de ratón y biotecnólogo, a la actual crisis sanitaria en la que estamos instalados, causada por el nuevo coronavirus SARS-CoV-2, responsable de la enfermedad coronavírica (COVID-19). Y he recopilado diversas evidencias científicas y modelos animales para el estudio de la patogénesis y el desarrollo de terapias contra estos coronavirus que puede que encontréis interesantes. A continuación describiré la generación y el uso de diversos modelos animales, ratones transgénicos, para el estudio de la infección causada por diferentes coronavirus que afectan a los humanos.
Para empezar una obviedad creo importante. Toda terapia o tratamiento que queramos administrar a seres humanos deberá seguir un protocolo bien conocido y establecido. Este procedimiento empieza siempre con experimentos de investigación básica, en laboratorios de investigación en centros y universidades, y suele implicar el uso de modelos celulares, o bien con células animales o bien ya con células humanas en cultivo. Sí se descubre algún mecanismo o proceso que pueda tener una trascendencia terapéutica entonces habrá que continuar la investigación con modelos animales, experimentando con ellos, en lo que se conoce como la fase pre-clínica de un proyecto de investigación. Los experimentos con animales siguen siendo necesarios para validar la seguridad (la no toxicidad) y posible eficacia pre-clínica de una propuesta terapéutica experimental, antes de empezar a administrar ese tratamiento en humanos. Es importante que todos sepamos lo estrictamente regulada que está la experimentación animal, que solo se aplica si no hay otro método alternativo, y lo absolutamente necesarios que siguen siendo en investigación biomédica. Finalmente, superadas todas las fases anteriores, se llega a los ensayos clínicos, ya con personas, con sus sucesivas fases (I, II, III, IV) hasta que se comprueba que el tratamiento es seguro y eficaz en seres humanos, y entonces las autoridades revisan toda esta información y pueden conceder la autorización correspondiente, para que la propuesta original se convierta en un tratamiento, que ya podrá administrarse en cualquier hospital. La duración de todo este proceso suele ser larga, alrededor de un año, como mínimo, y frecuentemente muchos más, aunque en determinados casos puedan acortarse algunas etapas, por razones de interés sanitario o de uso compasivo. Eso explica que se anuncien posibles propuestas de vacunas para el nuevo coronavirus que todavía tardarán bastantes meses en llegar a la práctica clínica habitual.
Ahora que tenemos ya claro que los animales de laboratorio, como los ratones, son muy importantes en la investigación biomédica, la siguiente pregunta es saber si el modelo animal más extendido en todos los laboratorios (el ratón) es infectable por el coronavirus causante del COVID-19. La respuesta es no. De forma natural, el coronavirus SARS-CoV-2 no infectará a las células del ratón, como sí infecta nuestras células. La razón la hemos conocido a principios del mes de marzo, gracias a un estudio publicado en la revista Cell, que demuestra que el nuevo coronavirus SARS-CoV-2 accede al interior de nuestras células a través de una proteína de membrana llamada ACE2 (Angiotensin-Converting enzyme 2), que actua como receptor al cual se une la proteína S (Spike, espícula de la corona) del coronavirus, y cuya estructura atómica ya comentó Francis Villatoro en su blog. Esta infografía publicada en Materia-El País por Arturo Galocha y Nuño Domínguez ilustra muy bien como entre el coronavirus en nuestras células. La proteína ACE2 es el mismo receptor que usaba el coronavirus SARS-CoV que apareció en 2002 y causó el Síndrome Respiratorio Severo Agudo (en inglés, SARS). El descubrimiento de este receptor puede dar paso al desarrollo de anticuerpos bloqueantes anti-ACE2 y/o moléculas que impidan la unión de la proteína S del virus al receptor, o, como también indican en el mismo estudio, para desarrollar inhibidores de una proteasada llamada TMPRSS2 que actúa a continuación procesando la proteína S y rompiéndola en fragmentos activos de tamaño más pequeño.

La proteína Ace2 de los ratones es distinta a la proteína ACE2 humana, por eso ni el coronavirus SARS-CoV ni el actual SARS-CoV-2 pueden infectar a los ratones. Eso impediría usar a estos roedores como modelos animales para la investigación de la infección por estos coronavirus. A no ser que transformáramos al ratón, lo alteráramos genéticamente, y lo convirtiéramos en susceptible de ser infectable por estos dos coronavirus. Eso es exactamente lo que hicieron en la Universidad de Iowa (EE.UU.) en 2007, generando unos ratones transgénicos que expresan el gen humano ACE2 bajo el control del promotor y las regiones reguladoras del gen K18 (queratina 18), que dirigen la expresión específicamente a las células epiteliales. Estos ratones trangénicos K18-hACE2 ahora sí que son infectables por coronavirus SARS-CoV y son capaces de provocar una rápida letalidad (menos de una semana) tras inocularles intranasalmente el coronavirus.
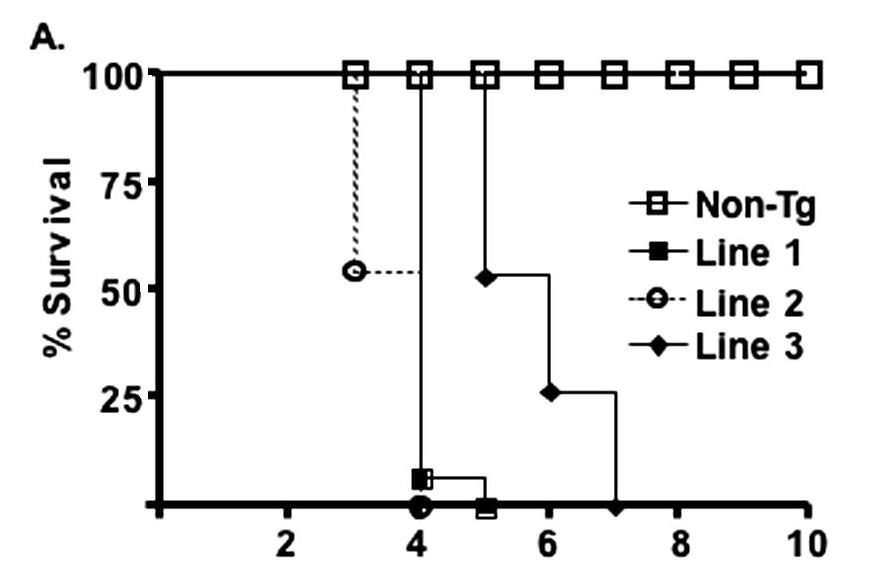
Estos ratones transgénicos K18-hACE2 ya tienen la proteína humana ACE2 que el virus necesita para entrar en las células del ratón, y por eso se convirtieron en su momento (y siguen siendo) un estupendo modelo animal para investigar la infección de estos ratones por SARS-CoV, los mecanismos que permiten que esta infección ocurra y, en especial, para desarrollar y validar vacunas y terapias anti-virales efectivas.
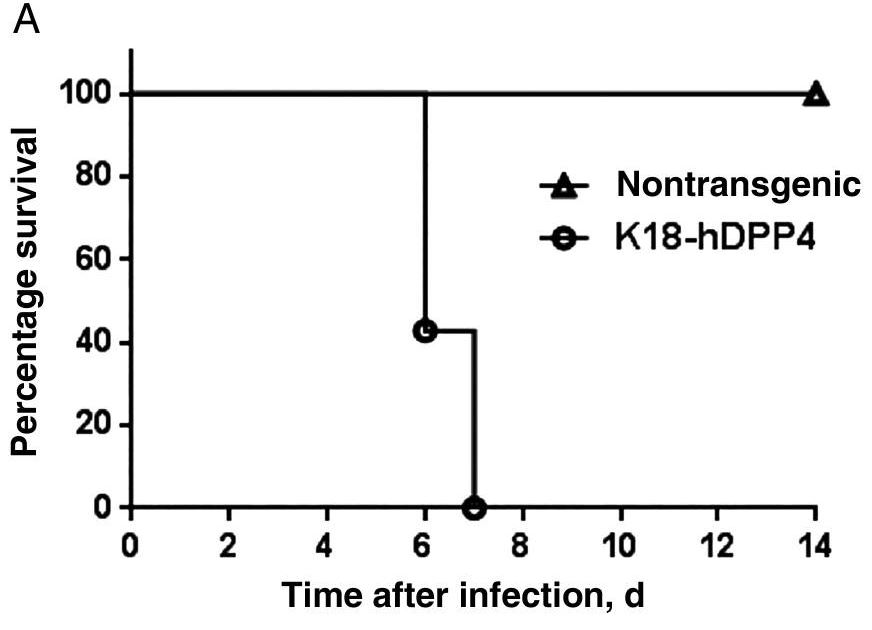
Posteriormente, cuando surgió el coronavirus MERS-CoV, en 2012, que afectó principalmente a varios países de Oriente Medio, principalmente a la península arábiga, con una mortalidad muy elevada, cercana al 30% de los infectados, se descubrió que este coronavirus accedía a las células humanas a través del receptor DDP4 (dipeptidil peptidasa 4) en la superficia de las células. Algunos años después, el mismo equipo investigador de la Universidad de Iowa (EE.UU.) generó otro modelo animal, un nuevo ratón transgénico que expresaba el gen humano hDPP4 bajo el control del promotor y zonas reguladoras del gen K18. Los ratones trangénicos resultantes, K18-hDPP4, también fallecían a los 7 días después de ser inoculados intranasalmente con el coronavirus MERS-CoV.
¿Tenemos algún modelo animal disponible para el nuevo coronavirus SARS-CoV-2 ? Naturalmente. El mismo modelo animal que era útil para investigar el SARS-CoV precedente sigue siéndolo para investigar ahora el SARS-CoV-2, dado que ambos virus comparten el mismo receptor de entrada a la célula: la proteína ACE2. Por eso, los ratones transgénicos K18-hACE2 se han convertido en un modelo animal muy deseado y solicitado por todos aquellos investigadores que investigan la patogenicidad de este nuevo virus, y las posibles terapias que se puedan desarrollar para luchar contra esta infección causante del COVID-19. Estos ratones están actualmente disponibles desde uno de los mayores repositorios internacionales de modelos de ratón: The Jackson Laboratory. Esta es la ficha de estos ratones K18-hACE2 en Jax.
Sin embargo, frecuentemente la biología es más compleja de lo que suponemos y no deja de sorprendernos. Un equipo de investigadores chinos acaba de depositar un manuscrito en el servidor público bioRxiv de pre-prints, en el que demuestran que el coronavirus SARS-CoV-2 no solo parece entrar en las células humanas a través de la proteína/receptor ACE2 sino que también lo hace a través de la proteína CD-147 (también llamada Basigina, BSG). En el mismo estudio los autores igualmente demuestran que el uso de anticuerpos bloqueantes anti-CD-147 inhiben la capacidad infectiva del coronavirus SARS-CoV-2 en células humanas en cultivo. Si se confirma esta observación (el manuscrito todavía no ha sido evaluado por pares ni publicado formalmente en ninguna revista) obligaría a revisar las expectativas terapéuticas que se habían lanzado para bloquear la vía de acceso a través de ACE2, dado que el coronavirus siempre tendría una puerta alternativa, una puerta trasera (la proteína CD-147/BSG) que podría usar para acceder al interior de las células humanas.

¿Disponemos ya de algún modelo animal, de algún ratón transgénico o mutante que pueda usarse para investigar la vía de entrada del coronavirus a través de BSG? Sí, hay varios modelos animales disponibles. A pesar de que algunos de los ratones mutante (knock-out) del gen murino Bsg manifiestan letalidad perinatal o problemas de fertilidad, existen otros ratones mutantes condicionales que solamente inactivan el gen Bsg en fibroblastos, perfectamente viables. Y, lo que es más importante, se han desarrollado otros ratones mutantes knock-in en el que se les ha substituido el gen murino Bsg por el gen humano BSG. Este es un ejemplo de ratón «humanizado» en el que un gen murino ha sido reemplazado por su equivalente humano. Por lo tanto estos últimos ratones mutantes humanizados ya son infectables por el nuevo coronavirus y también pueden usarse para investigar la patogenicidad y el desarrollo de terapias contra SARS-CoV-2.
Este artículo es un pequeño resumen que sirve para ilustrar la relevancia de los modelos animales, como los ratones modificados genéticamente, en la investigación de las infecciones causadas por los coronavirus que infectan a seres humanos.
Nota añadida el 12 de abril de 2020
Recientes estudios han confirmado que tanto los gatos (felinos) como los hurones (mustélidos) pueden infectarse con el coronavirus SARS-CoV-2. Por el contrario, no parece tan fácil que este virus consiga replicarse en los perros, cerdos, pollos y patos. En particular, la infección que causa el SARS-CoV-2 a los hurones es muy parecida al COVID-19 y recapitula los síntomas detectados en seres humanos. Por eso, el uso de hurones permite disponer ahora de un modelo animal adicional (además de los ratones transgénicos mencionados anteriormente) para poder investigar estrategias de bloqueo y/o progreso de la infección mediante antivirales o vacunas, en estos animales.
Una versión de este artículo se ha publicado posteriormente en The Conversation el 16 de marzo de 2020.


6 Comentarios